OBJETIVO:
Analizar las propiedades químicas que existen en diferentes analgésicos.
HIPÓTESIS:
Analgésico (5 diferentes)---- medir ---> PH
---> Solubilidad
---> composición e interacción
MATERIAL:
*Papel pH
*apel encerado
*5 tubos de ensaye
*2 hojas de papel blanco
*3 frascos goteros
*Gradilla
*5 Tabletas de una marca comercial
*Pastillas de diferente marca
PROCEDIMIENTO:
1.-Comparación de pH entre diferentes marcas de analgésicos.
2.-Muela dos tabletas de una de las marcas.
3.-Ya molidas agréguelas en 15 mL de agua en un tubo de ensayo.
4.-Mezcle bien agitando la disolución en el tubo de ensayo.
5.-Haga lo mismo con cada una de las tabletas de las diferentes marcas que haya traído.
6.- marque los tubos para diferenciarlos.
7.-Mida la acidez de cada marca de aspirina con el papel pH y anote el valor de pH registrado para cada marca.
8.-Tire las disoluciones en la tarja y deje que fluya un poco el agua.
9.-Comparación del tiempo requerido para disolver las tabletas de analgésico en ácido.
1O.-Pon una tableta de cada analgésico en un tubo de ensayo en una gradilla y agrégale 3 mL de ácido clorhídrico 1M en cada tubo.
11.-Sin agitar, anota el tiempo que tarda en disolver cada tableta.
12.-Hay algunos componentes de la aspirina que no son solubles, considere el tiempo en que la mayor parte de la tableta se disuelva.
13.-Registre cual producto se disolvió más rápido y revise las etiquetas ver en qué difiere cada producto.
14.-Tire las disoluciones en la tarja y deje fluir un poco de agua.
Análisis de la composición de las tabletas de analgésico:
Las hojas de papel blanco divídalas en nueve secciones y anote en cada sección los nombres: almidón, azúcar, talco, ácido salicílico, los nombres de tres productos analgésicos comerciales y la aspirina que envejeció; corte como etiquetas cada sección.
Sobre el papel encerado coloque las etiquetas y agregue aproximadamente una cucharadita de cada sustancia junto a su etiqueta. Habrá un montoncito de cada sustancia en cada hoja de papel encerado. Las tabletas deberán molerse.
En cada una de las sustancias de una hoja encerada agregue de 1 a 2 gotas de tintura de yodo en una de las pilas de cada sustancia y observe si hay o no-reacción. Anote cualquier observación, especialmente cambios de color.
En cada una de las sustancias de la otra hoja de papel encerado agregue 1 a 2 gotas de la disolución de cloruro férrico sobre la pila remanente de cada sustancia y observe si hay o no-reacción. Anote cualquier observación, especialmente cambios de color.
OBSERVACIONES:
Al agregar tintura de Yodo en las sustancias, las gotas se empolvaron y se encapsularon en esferas de agua y al agregar cloruro de fierro algunas adquirieron un color diferente, se volvieron mas flexibles y consistentes.
Los medicamentos de marcas prestigiosas o un poco mas caros poseen mas propiedades que los baratos.
Aunque la composición sea la misma entre el medicamento de una marca y otra hay diferencias las cuales provienen de los procesos que se utilicen para hacer el medicamento
En el analgésico ibuprofeno de pflizer se observaron diversos cambios de color negro/morado/café al agregarse cloruro de fierro.
Los analgésicos poseen diferentes propiedades según sea su composición.
ANÁLISIS:
CONCLUSIÓN:
Los medicamentos han cambiado mucho la vida de los humanos, los analgésicos como la aspirina se han vuelto muy populares debido a sus beneficios y su producción a bajo costo. Cada analgésico y cada medicamento posee diversas propiedades las cuales son diferentes entre unos y otros, estas características pueden ser observadas mediante diversas reacciones y así se puede comprobar la diferencia entre medicamentos.
jueves, 5 de mayo de 2011
PEGAMENTO CON LECHE.
OBJETIVO:
Hacer resistol con leche &vinagre.
HIPOTESIS: Leche + vinagre --- calor ---> liquido grumoso ---> al filtrarse da pegamento.
MATERIAL:
*1 vaso de precipitados de 250 mL
*Papel filtro
*Mechero bunsen
*Cartón
*Madera
*Embudo
*¼ lt. De leche descremada
*Bicarbonato de sodio
*2 o 3 cucharadas de vinagre de alcohol.
PROCEDIMIENTO:
1.-Coloca la leche en un vaso de precipitados.
2.-Agrégale el vinagre de alcohol.
3.-Calienta muy lentamente la leche con el vinagre, remueve con un agitador, hasta que formen pequeños grumos.
4.-Retira el vaso del fuego.
5.-Continúa removiendo hasta que no se formen nuevos grumos.
6.-Deje el vaso en reposo para que se enfríe y para que precipite el sólido (cuajo) y se separe del líquido (suero).
7.-Separa el sólido filtrando la mezcla con el papel filtro.
8.-Exprime suavemente eliminar el líquido del papel.
9.-Enjuaga el sólido con agua destilada y coloca el sólido en un vaso de precipitados.
1O.-Agrégale ½ cucharada de bicarbonato de sodio, para neutralizar el exceso de ácido que pueda haber quedado. Observa la formación de las burbujas de CO2.
11.-Agrega bicarbonato hasta que no se forme burbujas.
12.-Prueba las características del pegamento obtenido pegando papeles, trozos de madera lisa, etc.
13.-Si tiene pegamento comercial en base de caseína compare las propiedades adhesivas de ambos.
14.-El pegamento una vez seco, es resistente a la acción de la humedad. Para ello, pega dos trozos de madera y deja secar, luego introduce el material en agua y observa si se mantienen unidos.
OBSERVACIONES:
Al poner a herbir el vinagre con la leche comenzó a cortarse y a desprender un fuerte olor además de que se separo en dos faces sólida y líquida.
Al filtrar la fase sólida de la líquida el sólido se hizo espeso y al agregarse el bicarbonato de sodio comenzó a desprender CO2 en forma de burbujas lo que hizo que se esponjara el pegamento y obtuviera una consistencia espesa y de color blanca uniforme, además del olor característico del pegamento blanco.
ANÁLISIS:
El resistol obtenido tiene una consistencia espesa, más sólida que líquida, posee características que le permiten mantener unidos trozos de madera papel y cartón. Para su obtención se puso a reaccionar 1/4 de leche con 3 cucharadas de vinagre (acido acético) más calor y luego se neutralizo con el CO2, los grumos que había cuando hirvió fueron los que posteriormente formaron el resistol.
CONCLUSIÓN:
El pegamento que hicimos en esta práctica es un polímero hecho a partir de las propiedades de la leche y pudo hacerse gracias al vinagre y la reacción que tuvo al ponerse a hervir dando como resultado un líquido blanco homogéneo listo para pegar objetos como madera y cartón demostrando así que los polímeros son útiles en la vida cotidiana y pueden utilizarse como impermeables, protección de objetos o para pegar cosas como es el caso del pegamento.
Hacer resistol con leche &vinagre.
HIPOTESIS: Leche + vinagre --- calor ---> liquido grumoso ---> al filtrarse da pegamento.
MATERIAL:
*1 vaso de precipitados de 250 mL
*Papel filtro
*Mechero bunsen
*Cartón
*Madera
*Embudo
*¼ lt. De leche descremada
*Bicarbonato de sodio
*2 o 3 cucharadas de vinagre de alcohol.
PROCEDIMIENTO:
1.-Coloca la leche en un vaso de precipitados.
2.-Agrégale el vinagre de alcohol.
3.-Calienta muy lentamente la leche con el vinagre, remueve con un agitador, hasta que formen pequeños grumos.
4.-Retira el vaso del fuego.
5.-Continúa removiendo hasta que no se formen nuevos grumos.
6.-Deje el vaso en reposo para que se enfríe y para que precipite el sólido (cuajo) y se separe del líquido (suero).
7.-Separa el sólido filtrando la mezcla con el papel filtro.
8.-Exprime suavemente eliminar el líquido del papel.
9.-Enjuaga el sólido con agua destilada y coloca el sólido en un vaso de precipitados.
1O.-Agrégale ½ cucharada de bicarbonato de sodio, para neutralizar el exceso de ácido que pueda haber quedado. Observa la formación de las burbujas de CO2.
11.-Agrega bicarbonato hasta que no se forme burbujas.
12.-Prueba las características del pegamento obtenido pegando papeles, trozos de madera lisa, etc.
13.-Si tiene pegamento comercial en base de caseína compare las propiedades adhesivas de ambos.
14.-El pegamento una vez seco, es resistente a la acción de la humedad. Para ello, pega dos trozos de madera y deja secar, luego introduce el material en agua y observa si se mantienen unidos.
OBSERVACIONES:
Al poner a herbir el vinagre con la leche comenzó a cortarse y a desprender un fuerte olor además de que se separo en dos faces sólida y líquida.
Al filtrar la fase sólida de la líquida el sólido se hizo espeso y al agregarse el bicarbonato de sodio comenzó a desprender CO2 en forma de burbujas lo que hizo que se esponjara el pegamento y obtuviera una consistencia espesa y de color blanca uniforme, además del olor característico del pegamento blanco.
ANÁLISIS:
El resistol obtenido tiene una consistencia espesa, más sólida que líquida, posee características que le permiten mantener unidos trozos de madera papel y cartón. Para su obtención se puso a reaccionar 1/4 de leche con 3 cucharadas de vinagre (acido acético) más calor y luego se neutralizo con el CO2, los grumos que había cuando hirvió fueron los que posteriormente formaron el resistol.
CONCLUSIÓN:
El pegamento que hicimos en esta práctica es un polímero hecho a partir de las propiedades de la leche y pudo hacerse gracias al vinagre y la reacción que tuvo al ponerse a hervir dando como resultado un líquido blanco homogéneo listo para pegar objetos como madera y cartón demostrando así que los polímeros son útiles en la vida cotidiana y pueden utilizarse como impermeables, protección de objetos o para pegar cosas como es el caso del pegamento.
martes, 3 de mayo de 2011
¿Qué es un principio activo?
OBJETIVO:
Sintetizar ácido acetilsalicílico (aspirina) &salicilato de metilo.
HIPÓTESIS:
Ácido salicilico + anhídrido acético + ácido sulforico ------------ ácido acetilsalicilico.
Ácido salicilico + ácido sulfurico + alcohol metílico ------------- salicilato de metilo.
MATERIAL:
*2 tubos de ensayo.
*1 pipeta beral
*Pinzas para tubo de ensaye
*Mechero bunsen
*Embudo y papel filtro
*1 soporte universal completo
*1 vaso de precipitados de 250 mL
*Lentes
*1 gr. de ácido salicílico
*20 mL de agua fría
*20 mL de ácido sulfúrico concentrado (H2SO4)(18M)
*50 mL de alcohol metílico
*20 mL de anhí-drido acético concentrado
*Hielo
PROCEDIMIENTO:
1.- Ponga 0.5 gr. de ácido salicílico en un tubo de ensayo.
2.- Agregue aproximadamente 1 mL de anhídrido acético y mezcle agitando el tubo de ensaye.
3.- En la pipeta beral tome ácido sulfúrico concentrado y agregue una gota al tubo de ensayo.
4.- En el vaso de precipitados caliente agua (hasta 500C) para utilizarlo como baño maría, en él ponga el tubo de ensayo en el baño de agua. Evite que entre agua al tubo de ensayo, ya que interfiere en la reacción.
5.- Retire con unas pinzas el tubo de ensayo e introdúzcalo en un vaso con hielo.
6.- Agregue aproximadamente 2 mL de agua helada al tubo de ensayo en el baño de hielo.
7.- Deje el tubo de ensayo hasta que se formen los cristales.
8.- Recoja los cristales de ácido acetilsalicílico crudo extrayendo el exceso de disolvente con una pipeta plástica (beral) o filtre.9.- Lave los cristales dos veces con una pequeña cantidad de agua helada, quitando el exceso de agua con una pipeta después de cada lavado.
1O.- Vacíe el sólido del tubo de ensayo a un pedazo de papel filtro o toalla de papel para que se seque.
Preparación de SALICILATO DE METILO
1.- En un tubo de ensaye ponga 0.5 gr. de ácido salicílico.
2.- Anote sus observaciones.
3.- Tome con la pipeta beral alcohol metílico, agregue con cuidado 3 mL (60 gotas) y una gota de ácido sulfúrico concentrado.
4.- Mezcle bien agitando el tubo suavemente.
5.- Caliente la mezcla en un baño de agua hirviendo por 15 minutos.
ANÁLISIS:
El acido salicilico producto de la corteza de sauce blanco puede sintetisarce &producir analgésicos para diversos dolores &tros problemas, la síntesis de diversos principios activos conlleva el uso de diversos químicos que dan como reactivo un producto que debe purificarse &tratarse para poder ser comestibles.
El uso de medicamentos debe de ser prescrito ya que puede haber reacciones alérgicas o intoxicaciones si no se toma la dosis adecuada.
OBSERVACIONES:
*Cuando se realiza la reacción para la formación de aspirinas debe de haber un cambio brusco de temperatura de caliente a fría para poder cristalizarse el ácido acetilsalicilico.
*El acido salicilico es muy impregnante al olfato & nos causo picor en la nariz.
*El salicilato de metilo es un analgesico topico que desprende un olor aromático agradable debido a que en su sintetización se utiliza alcohol metílico.
CONCLUSIÓN:
El ácido salicílico es aditivo clave en muchos productos &en anestesicos su descubrimiento se remonta a las antiguas culturas egipcias & griega que extraían del sauce blanco el polvo que hoy conocemos como ácido salicílico &que en el siglo XIX pudo ser sintetizado a acido acetilsalicílico y que su uso es de amplio espectro en la actualidad conocido simplemente como aspirina.
lunes, 2 de mayo de 2011
TAREA DE LOS MEDICAMENTOS.
Un medicamento es toda sustancia medicinal y sus asociaciones o combinaciones destinadas a su utilización en las personas o en los animales que se presente dotada de propiedades para prevenir, diagnosticar, tratar, aliviar o curar enfermedades o dolencias o para afectar a funciones corporales o al estado mental.
También se consideran medicamentos las sustancias medicinales o sus combinaciones que pueden ser administrados a personas o animales con cualquiera de estos fines aunque se ofrezcan sin explícita referencia a ellos.
CLASIFICACIÓN:
Los medicamentos se dividen en 5
* Especialidad farmacéutica: Es el medicamento de composición e información definidas, de forma farmacéutica y dosificación determinadas, preparado para su uso medicinal inmediato, dispuesto y acondicionado para su dispensación al público, con denominación, embalaje, envase y etiquetado uniformes según lo dispongan las autoridades sanitarias.
* Fórmula magistral: Es el medicamento destinado a un paciente individualizado, preparado por el farmacéutico, o bajo su dirección, para cumplimentar expresamente una prescripción facultativa detallada de las sustancias medicinales que incluye, según las normas técnicas y científicas del arte farmacéutico, dispensado en su farmacia o servicio farmacéutico y con la debida información al usuario.
* Preparado o fórmula oficinal: Es aquel medicamento elaborado y garantizado por un farmacéutico o bajo su dirección, dispensado en su oficina de farmacia o servicio farmacéutico, enumerado y descrito por el Formulario, destinado a la entrega directa a los enfermos a los que abastece dicha farmacia o servicio farmacéutico.
* Medicamento prefabricado: Es el medicamento que no se ajusta a la definición de especialidad farmacéutica y que se comercializa en una forma farmacéutica que puede utilizarse sin necesidad de tratamiento industrial y al que la autoridad farmacéutica otorgue autorización e inscriba en el registro correspondiente.
* Medicamento en investigación: Forma farmacéutica de una sustancia activa o placebo, que se investiga o se utiliza como referencia en un ensayo clínico, incluidos los productos con autorización de comercialización cuando se utilicen o combinen, en la formulación o en el envase, de forma diferente a la autorizada, o cuando se utilicen para tratar una indicación no autorizada, o para obtener más información sobre un uso autorizado.
PRINCIPIO ACTIVO.
Un principio activo o ingrediente activo ("Active ingredient", en inglés) es aquella sustancia con actividad farmacológica extraída de un organismo vivo que una vez purificada y/o modificada químicamente, se le denomina fármaco o medicamento.
El Real Decreto 1345/2007, de 11 de octubre, por el que se regula el procedimiento de autorización, registro y condiciones de dispensación de los medicamentos de uso humano fabricados industrialmente define al principio activo como:
“toda materia, cualquiera que sea su origen -humano, animal, vegetal, químico o de otro tipo- a la que se atribuye una actividad apropiada para constituir un medicamento”.
EXCIPIENTE.
En farmacéutica, un excipiente es una sustancia activa usada para incorporar el principio activo. Además pueden ser usados para ayudar al proceso mediante el cual un producto es manufacturado.
Tipos de excipientes
* Atadores (binders): mantienen los ingredientes de una tableta unidos; Comúnmente se utilizan Almidones, azúcares y celulosas como Hidroxipropil celulosa o lactosa. También se utilizan azúcares alcohólicas como Xilitol, sorbitol o maltitol.
* Rellenos (Fillers): rellenan el contenido de una pastilla o cápsula para lograr una presentación conveniente para el consumo. La celulosa vegetal es un relleno cuyo uso es bastante extendido en tabletas o cápsulas de gelatina dura. El fosfato de calcio dibásico es también un relleno popular para tabletas. Para cápsulas de gelatina blanda suele utilizarse flor de cártamo (de la cual México es el principal productor mundial).
* Desintegradores (disintegrants): estos se expanden y disuelven cuando se les moja, así causando que la tableta se rompa en el tracto digestivo y libere los nutrientes para su absorción.
* Lubricantes (lubricants): previenen que los ingredientes se agrupen en terrones o que se peguen en alguna de las máquinas industriales con los que se fabrican. Los minerales comunes como talco o silica, y grasas esteroides son los lubricantes más frecuentes en tabletas o cápsulas de gelatina dura.
* Recubridores (coatings): protegen los ingredientes de la tableta de los efectos del aire, de la humedad y ayudan a que las tabletas de sabor poco placentero sean más fáciles de tragar. La mayoría de las tabletas recubiertas utilizan una capa de celulosa (fibra vegetal) que está libre de sustancias alergénicas. Otros materiales utilizados son polímeros sintéticos u otros polisacáridos. Según la velocidad de disolución de un recubrimiento se puede determinar en que lugar del tracto digestivo se liberen las proteínas, o el periodo de acción de estas.
* Endulzadores: sirven para hacer las pastillas más deglutibles, otorgándoles sabor más agradable.
* Saborizantes y colorizantes: son para mejorar la presentación pública de un medicamento.
5 MEDICAMENTOS CON SU COMPOSICIÓN.
BUSCAPINA COMPOSITUM*
BUTILHIOSCINA
METAMIZOL
PARACETAMOL
FORMA FARMACÉUTICA Y FORMULACIÓN
Cada ml contiene:
Bromuro de butilhioscina........ 6.670 mg
Metamizol............................... 333.400 mg
Vehículo, c.b.p. 1 ml.
Cada ampolleta contiene:
Bromuro de butilhioscina........ 20.00 mg
Metamizol........................................... 2.5 g
Vehículo, c.b.p. 5 ml.
Cada GRAGEA contiene:
Bromuro de butilhioscina............ 10 mg
Metamizol sódico........................ 250 mg
Excipiente, c.b.p. 1 gragea.
TEMPRA FORTE*
PARACETAMOL
FORMA FARMACÉUTICA Y FORMULACIÓN
Cada GRAGEA contiene:
Paracetamol DC 90 equivalente a ...................... 650 mg
de paracetamol
Excipiente, c.b.p. .................................................... 1 gragea
LORATADINA*
FORMA FARMACÉUTICA Y FORMULACIÓN:
JARABE
Loratadina.................................................................. 5 y 100 mg
SOLUCIÓN
Loratadina....................................................................... 100 mg
TABLETAS
Loratadina......................................................................... 10 mg
CIPRAÍN*
CIPROFLOXACINO
FORMA FARMACÉUTICA Y FORMULACIÓN
Cada TABLETA recubierta contiene:
Clorhidrato de ciprofloxacino monohidratado equivalente a .............................. 250 y 500 mg
de ciprofloxacino
Excipiente, c.b.p. 1 tableta.
ANALGEN*
NAPROXENO
FORMA FARMACÉUTICA Y FORMULACIÓN
Cada TABLETA contiene:
Naproxeno sódico........................... 220 mg
Excipiente, c.b.p. 1 tableta.
martes, 26 de abril de 2011
PRÁCTICA: ELABORACIÓN DE QUESO.
Objetivo:
Hacer queso y analizar sus componentes químicos.
Hipótesis:
Hacer queso<queso <reaccion xantoproteica,biuret y reconocimiento de lipidos
<suero <identificación de PH, glúcidos, proteínas lactalbumicas &lactoglobulina.
Material:
*1vaso de presipitado de 1000ml
*Bureta de 250ml
*Mechero de bunsen
*1 termometro
*2 vasos de presipitado uno de 250ml y otro de 50ml
*Soporte universal completo
*Cuchillo
*1m2 de manta
*Canasta
*Cuchara de madera
*Probeta de 100ml
*1 litro de leche
*Disolución de cloruro de calcio al 50%
*Agua destilada
*Cloruro de sodio
*Cuajo líquido
*Disolución 0.1M de NaOH
*Indicador universal
*Papel PH
Procedimiento:
Pusimos a calentar a 37°C 500ml de leche.
Se agregaron 10ml de disolución de Cloruro de Calcio y se revolvió.
Se agregaron 3 gotas de cuajo liquido y se dejó reposar 30 min.
Se separo el suero del queso utilizando la manta y se exprimio esta para que en su interior quedara el queso.
Análisis del suelo.
Se analizó el nivel de PH que fue menor a 7, es ácido.
En un tubo con 10ml de suero se agregó indicador universal.
Después agregamos gota a gota la disolución de 0.1M de NaOH en el suero, se agito para homogeneizar cuando cambio a verde indicó la neutralizacion, cantidad de NaOH 0.1 = 5 gotas
Observaciones:
Al momento de que se fermentaba, la mezcla se ponía caliente cada vez mas, esto fue gracias a la reacción de fermentación.
La formación de queso depende del tipo de leche que se ocupe, entre mas procesada sea el queso será en menor cantidad y menos sólido.
Al fermentarse la leche da como resultado varios productos con bacterias benéficas para los seres humanos.
Conclusión:
Las fermentaciones son posesos llevados acabo por bacterias y los medios necesarios para que estas proliferen y si las condiciones son alimentos que poseen ciertas características el producto fermentado puede ser comestible e incluso benéfico para quien lo consume.
Hacer queso y analizar sus componentes químicos.
Hipótesis:
Hacer queso<queso <reaccion xantoproteica,biuret y reconocimiento de lipidos
<suero <identificación de PH, glúcidos, proteínas lactalbumicas &lactoglobulina.
Material:
*1vaso de presipitado de 1000ml
*Bureta de 250ml
*Mechero de bunsen
*1 termometro
*2 vasos de presipitado uno de 250ml y otro de 50ml
*Soporte universal completo
*Cuchillo
*1m2 de manta
*Canasta
*Cuchara de madera
*Probeta de 100ml
*1 litro de leche
*Disolución de cloruro de calcio al 50%
*Agua destilada
*Cloruro de sodio
*Cuajo líquido
*Disolución 0.1M de NaOH
*Indicador universal
*Papel PH
Procedimiento:
Pusimos a calentar a 37°C 500ml de leche.
Se agregaron 10ml de disolución de Cloruro de Calcio y se revolvió.
Se agregaron 3 gotas de cuajo liquido y se dejó reposar 30 min.
Se separo el suero del queso utilizando la manta y se exprimio esta para que en su interior quedara el queso.
Análisis del suelo.
Se analizó el nivel de PH que fue menor a 7, es ácido.
En un tubo con 10ml de suero se agregó indicador universal.
Después agregamos gota a gota la disolución de 0.1M de NaOH en el suero, se agito para homogeneizar cuando cambio a verde indicó la neutralizacion, cantidad de NaOH 0.1 = 5 gotas
Observaciones:
Al momento de que se fermentaba, la mezcla se ponía caliente cada vez mas, esto fue gracias a la reacción de fermentación.
La formación de queso depende del tipo de leche que se ocupe, entre mas procesada sea el queso será en menor cantidad y menos sólido.
Al fermentarse la leche da como resultado varios productos con bacterias benéficas para los seres humanos.
Conclusión:
Las fermentaciones son posesos llevados acabo por bacterias y los medios necesarios para que estas proliferen y si las condiciones son alimentos que poseen ciertas características el producto fermentado puede ser comestible e incluso benéfico para quien lo consume.
lunes, 25 de abril de 2011
Práctica del Pan.
Hipótesis:
El cuerpo humano esta compuesto solamente de elementos químicos que contienen los alimentos que se consume diariamente, el pan no es la excepción contienen diversas propiedades que se pueden observar por diversos métdos como los que realizaremos.
Objetivo:
Analizar las propiedades quimicas del pan.
Material:
*Una gradilla
*6 tubos de ensalle
*1 mechero
*Pinzas para tubos
*Balanza
*3 pipetas y cristalizador.
Sustancias:
*agua destilada,
*Nitrato de Plata 0.1n
*Cloruro de bario 1n
*Nitrato de amonio 1n
*Hidroxido de sodio al 40%
*Sulfato de cobre
*Molibdato de amonio al 16%
*Acido nitrico concentrado
*Reactivo fehling a y b
*Lugol
*Hidroxido de amonio.
Procedimiento:
1.-Colocar un tubo de ensalle con pan y llevarlo al mechero
2.-Introducir un pan en el tubo de ensalle, añadir agua destilada esperar y agregar nitrato de plata, si hay precipitado hay cloruros.
3.-Introducir una miga en un tubo, añadir agua y cloruro de bario si hay precipitado hay fosfatos
4.-Poner en un tubo 1ml de feling a y b e introducir un trozo de pan y poner a baño maria hasta la reduccion del reactivo por la maltosa y glucosa
5.-Poner un trozo de pan y agregar 10ml de agua después calentarlo a baño maría hasta que aparezca una especie de engrudo
6.-En una solución del reactivo a y b de feling, se agrega el pan anterior y se agregan 3 gotas de lugol
7.-Tomar un trozo de pan amasarlo y frotar en una hoja de papel si hay manchas significara que hay lipidos
8.-Tomar un trozo de pan amasarlo debajo del chorro del agua recogiendo en una maya lo que caiga,hacer dos bolitas e introducirlas en tubos de ensalle.
9.-En el 1er tubo se añade 1ml de acido nitrico y calentar a baño maria
10.-Retira el exceso de ácido nítrico vacía en un vaso de agua con cal y ala bolita agregale hidroxido de amonio concentrado.
11.-En el segundo tubo de ensalle añade 1ml de hidróxido de sodio al 40% y 10 gotas de sulfato de cobre 0.1M agita y observa la reacción.
1.-Colocar un tubo de ensalle con pan y llevarlo al mechero
2.-Introducir un pan en el tubo de ensalle, añadir agua destilada esperar y agregar nitrato de plata, si hay precipitado hay cloruros.
3.-Introducir una miga en un tubo, añadir agua y cloruro de bario si hay precipitado hay fosfatos
4.-Poner en un tubo 1ml de feling a y b e introducir un trozo de pan y poner a baño maria hasta la reduccion del reactivo por la maltosa y glucosa
5.-Poner un trozo de pan y agregar 10ml de agua después calentarlo a baño maría hasta que aparezca una especie de engrudo
6.-En una solución del reactivo a y b de feling, se agrega el pan anterior y se agregan 3 gotas de lugol
7.-Tomar un trozo de pan amasarlo y frotar en una hoja de papel si hay manchas significara que hay lipidos
8.-Tomar un trozo de pan amasarlo debajo del chorro del agua recogiendo en una maya lo que caiga,hacer dos bolitas e introducirlas en tubos de ensalle.
9.-En el 1er tubo se añade 1ml de acido nitrico y calentar a baño maria
10.-Retira el exceso de ácido nítrico vacía en un vaso de agua con cal y ala bolita agregale hidroxido de amonio concentrado.
11.-En el segundo tubo de ensalle añade 1ml de hidróxido de sodio al 40% y 10 gotas de sulfato de cobre 0.1M agita y observa la reacción.
Observaciones:
Todas las reacciones que se realizan debén realizarse con cuidado, cuando el pan se quema queda el carbono sólido &los compuestos orgánicos se quedan, sólo el carbono muestra que los alimentos son compuestos orgánicos &por lo tanto los alimentos que se consumen es de lo que están compuestos ellos mismos &estos alimentos los consumimos para reponer y/o reaparar los componentes de nuestros cuerpos.
Análisis:
Cuestionario:
¿El pan es un alimento completo?
Parcialmente si, ya que no contiene vitaminas ni proteínas por lo que debe mezclarse con una comida completa.
¿Tiene vitaminas?
Normalmente no, sólo el enriquecido las contiene.
¿Qué da el enriquecimiento?
Vitaminas minerales &algunas proteínas
¿El pan tostado engorda menos que el fresco?
Si, porque al secarse pierde varias propiedades entre ellas las grasas solubles
¿Qué es el pan integral?
El pan que contiene la cascara de la semilla del trigo
¿Qué componente glucido contiene que no hay en el pan normal?
Glucosa o monosacaridos pues se los agregan en la elaboración del pan fortificado o dulce a mas del 10%
¿Cuál es su función en el cuerpo?
Darle energia &formar estructuras celulares &esqueléticas muy resistentes.
¿Qué componentes hay en el pan?
DULCE: almidón, lípidos, protidos, cloruros, carbono, fosfatos &glusidos.
SALADO: almidón, pocos lípidos &protidos cloruros &carbono.
¿Es igual el salado que el dulce?
No, el dulce contiene azucares &grasas.
¿Qué es la reacción xantoproteica &cual la del biuter?
Prueba para detectar aminoacidos aromáticos, el reactivo es acido nitrico concentrado &aparece una coloración amarilla al agregar un hidroxido el color cambia a anaranjado.
Biuret: Para detectar la presencia de proteínas &enlaces pepticos, esta hecho de NaOH 20% & CuSO 1% el reactivo cambia a violeta con las proteínas y al rosa con las polipeptidos cortos, el hidroxido de potacio KOH no participa pero proporciona el medio alcalino para que la prueba tenga lugar.
¿Qué alimentos se fermentan?
Objetivo:
Observar compuestos &propiedades de la fermentación de la leche.
Hipótesis:
Observar &analizar los solidos &el suero de la leche cortada para saber que compuestos tiene.
Material:
*Leche
*Limón
*Cuchillo
*Vaso de presipitado de 1000ml
*1 probeta de 100ml
*Mechero de Bunsen
*Termometro de Alcohol*Indicador universal
*Termometro de Alcohol*Indicador universal
*Soporte universal completo
*Mechero
*Mechero
*Cloruro de Calcio 50%
*Disolución 0.1M de NaOH
*2 Vasos de presipitado uno de 250ml y otro de 50ml
*Papel PH*2 Vasos de presipitado uno de 250ml y otro de 50ml
*1m de Manta
*Agua destilada
*Cloruro de sodio
Procedimiento:
1.-Vaciar 100ml de leche en un vaso de presipitado y agregarle jugo de limon esperar hasta que la leche se corte.
2.-Filtrar el suero de la parte solido
3.-Introduce el papel ph para ver el nivel de acides que es menor a 7 pues es un acido.
4.-Toma 10ml del suero y vacialo en un vaso de presipitado de 50ml agregandole gotas de indicador universal coloca una bureta y se llena de una disolucion 0.1m de NaOH
5.-Se procede a titular el suero agregando gota a gota la disolucion de NaOH sobre los 10ml del suero conforme agregues la disolucion de hidroxido de sodio se agita cuidadosamente el vaso para homogenizarla, cuando la disolucion cambia de verde se habra neutralizado se anoto la cantidad de hidroxido de sodio que agregaste al vaso, se realizan los calculos para conocer la concentración del acido que contiene el suero.
6.-Se mezcla 1ml de solucion feling a con b en otro tubo de ensalle se pone 1ml de suero y un ml de reactivo calentando a baño maría.
7.-Se agrega 1ml de hidroxido de sodio al 40% y 5gotas de sulfato de cobre 0.01m y se agita, sera color azul, en otro tubo se agregara 1ml de suero y la reacción anterior.
8.-Se toma una porción de caseina y se filtro hasta que quede bien seco.
9.-Coloca una porción de caseina lavada y seca mas acido nitrico y se calienta a baño maría agregándole un ml de hidroxido de amonio.
10.-Colocamos una porción de caseina mas 1ml de hidróxido de sodio al 40% y se agita, se agrega sulfato de cobre 0.01M y el color violáceo indicara la presencia proteica.
11.-Se toma una porción del solido, se agrega eter y se ponen en un papel filtro, cuando el éter se evapore aparecerá en el papel una mancha de grasa.
Observaciones:
Todas las reacciones tienen como objetivo identificar la presencia de ciertos compuestos que se anidan en ellas, como en la leche el limón hace que la leche se corte &se formen fermentos.Conclución:
Las diversas sustancias que hay en la leche hacen que al reaccionar con un acido como el limon cambie y se fermente ademas de poseer ciertas sustancia lo que la vuelve un alimento muy completo para los seres vivos en especial los mamiferos.
Las diversas sustancias que hay en la leche hacen que al reaccionar con un acido como el limon cambie y se fermente ademas de poseer ciertas sustancia lo que la vuelve un alimento muy completo para los seres vivos en especial los mamiferos.
Cuestionario:
¿Qué función tuvo la disolución de Cloruro de Calcio?
Cortar la leche al volverla acida
¿Para qué se agrega el cuajo?
Para poder cuajar y separar el suero del solido
¿Qué son las encimas?
Son sustancias nesesarias para poder vivir y que nos ayudan ademas de no ser iguales &algunas estan prescentes en la leche.
¿Qué es la fermentacion?
Porliferación de bacterias &desprendimiento de hidrógeno &hay butiricas, lácticas, aceticas &alcoholicas.
¿La fruta se fermenta?
Si, dejándola al aire libre pues el azúcar hace que proliferen las bacterias en ella &algunas generan alcohol.
¿Cuáles son los productos de las fermentaciones lácticas?
Leche, queso, yogur &crema
¿Hay oxidación &reducción en la fermentación?
Si, la hacen los microorganismos &las bacterias.
¿Cuál es el glusido de la leche?
La lactosa &se ha detectado glucosa en pocas cantidades.
¿Por qué se pone rojo el reactivo de fehling?
debido a la lactosa &glucosa presentes en la leche &la fermentación que llevan acabo.
¿Qué función tuvo la disolución de Cloruro de Calcio?
Cortar la leche al volverla acida
¿Para qué se agrega el cuajo?
Para poder cuajar y separar el suero del solido
¿Qué son las encimas?
Son sustancias nesesarias para poder vivir y que nos ayudan ademas de no ser iguales &algunas estan prescentes en la leche.
¿Qué es la fermentacion?
Porliferación de bacterias &desprendimiento de hidrógeno &hay butiricas, lácticas, aceticas &alcoholicas.
¿La fruta se fermenta?
Si, dejándola al aire libre pues el azúcar hace que proliferen las bacterias en ella &algunas generan alcohol.
¿Cuáles son los productos de las fermentaciones lácticas?
Leche, queso, yogur &crema
¿Hay oxidación &reducción en la fermentación?
Si, la hacen los microorganismos &las bacterias.
¿Cuál es el glusido de la leche?
La lactosa &se ha detectado glucosa en pocas cantidades.
¿Por qué se pone rojo el reactivo de fehling?
debido a la lactosa &glucosa presentes en la leche &la fermentación que llevan acabo.
Fabricación de Jabón Casero.
Fabricación de jabón casero.
El jabón ya era utilizado desde el año 2.800 a.C De esta época data un material jabonoso encontrado en unos cilindros de arcilla durante una excavación arqueológica en la ciudad de Babilonia. En estos cilindros había unas tallas que describían el proceso de hervir las grasas con ceniza, método ancestral de fabricación de jabón. Durante la edad media el jabón era un artículo muy caro, por lo que su empleo era limitado. Recién en el siglo XIX que se difundió el uso del jabón en Europa y luego en el resto del mundo. Tanto los jabones de tocador como los detergentes parten de la misma base, la diferencia está en que los jabones se fabrican a partir de sustancias nturales, como grasas animales y vegetales, mientras que los detergentes se elaboran a partir de materias primas sintéticas. El jabón es básicamente una sal obtenida de las grasas, que resulta soluble en el agua. La saponificación es la reacción de una solución alcalina con las grasas animales y vegetales (sebo y aceites)
Objetivo:
1.- No desperdiciar el aceite comestible que muchas veces sobra en la cocina.
Materiales:
· Aceite comestible usado de cualquier clase: soja, girasol, semillas, oliva. etc. Hay que pasarlo por un colador muy fino para quitarle las impurezas.
· Un Tacho plástico de pintura
· Palo de madera para revolver.
· Moldes de plástico o tergopol.
· Agua.
· Soda cáustica. (Hidróxido sódico).
· Sal común.
· Medio vaso de lavavajillas para darle aroma al jabón.
Procedimiento:
1.- Guardar el aceite usado hasta juntar dos litros y medio.
2.- Llenar un tacho con dos litros y medio de agua. Para fabricar panes de jabón de colores se puede añadir al agua colorante de tortas.
3.- En un ambiente ventilado y con la ayuda de un palo, diluir en el agua medio kilo de soda cáustica y un puñado de sal. Se producirá una reacción química "exotérmica" (calor) que requiere algunas horas hasta que se enfrié . La soda cáustica es un material que daña la piel si se pone en contacto directo con ella. Por eso es recomendable utilizar guantes y lentes protectores.
4.- Se vierte lentamente el aceite sobre la mezcla líquida llamada también "lejía cáustica", revolviendo en forma permanente (siempre para el mismo lado, porque de lo contrario se puede "cortar" el jabón). Se calienta la mezcla con mechero hasta alcanzar la temperatura de ebullición y se mantiene durante dos horas este tratamiento a los efectos de producir la "saponificación" de las grasas. Esta reacción química es la que combina el sodio de la lejía con los ácidos grasos provenientes de los aceites para dar forma a una "sal orgánica soluble" que la conocemos como jabón. Si quiere hacer jabón con esencias añada hierbas aromáticas u otros tipos de aromas naturales después de que la mezcla bajo la temperatura a 40ºC.
5.- Cuando la mezcla se espesa, se echa en los moldes y se deja endurecer durante varios días. Si tiene ansiedad por ver como salen los jabones puede acelerar el proceso colocando algunos panes en el congelador.
6. Se sacan los jabones de los moldes. También se puede echar la mezcla en una bandeja grande. Se la deja reposar y antes de que se quede totalmente dura se corta en pastillas con un cortante común. Para que resulte más cómodo despegar los moldes se los puede enharinar o cubrir con aceite.
miércoles, 20 de abril de 2011
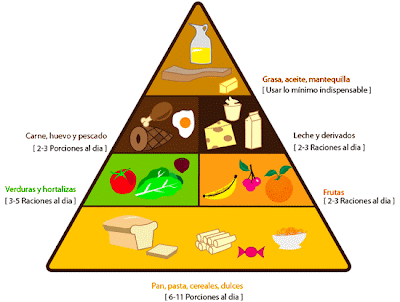
Ingesta Diaraia de Alimentos.
Para evitar los excesos y ausencias de los alimentos, se creó una "Piramide Alimenticia" en donde nos indican claramente cuánto y qué se debe de consumir diariamente.
Consumo de alimentos en 3 días.
Alimentos que consumí en 3 días:
| Día 1 | Día 2 | Día 3 |
| Mañana: licuado de plátano, galletas. Tarde: pollo con crema y chipotle, espagueti, sopa, agua natural, chocolate. Noche: leche y sándwich de jamón. | Mañana: licuado de mango, sándwich de jamón, galletas. Tarde: sopa, tacos dorados, frijoles, refresco. Noche: leche y pan. | Mañana: leche. Tarde: sándwich, licuado, pechuga empanizada, agua de naranja (natural). Noche: leche y pan. |
| Día 1 | Día 2 | Día 3 |
| Mañana: licuado de plátano (vitaminas A, B1, B2, B12, C y E) galletas (carbohidratos). Tarde: pollo con crema y chipotle (vitaminas), espagueti (proteínas), sopa (vitaminas), agua natural, chocolate (carbohidrato). Noche: leche (proteínas) y sándwich (cereales) de jamón (proteínas). | Mañana: licuado de mango, (vitaminas) sándwich (cereales) de jamón, (proteínas) galletas (carbohidratos). Tarde: sopa (vitaminas), tacos dorados, (cereales & algunas vitaminas) frijoles, (minerales) refresco (cafeína & azucares). Noche: leche (proteínas) y pan (carbohidratos). | Mañana: leche /proteínas). Tarde: sándwich, (cereales & vitaminas) licuado, (vitaminas) pechuga empanizada (vitaminas & ucarbohidratos), agua de naranja (natural). Noche: leche (proteínas) y pan (carbohidratos). |
Suscribirse a:
Comentarios (Atom)